
花药发育与花粉形成是开花植物有性生殖过程的重要环节,细胞核雄性不育(genic male sterility,GMS)基因是参与调控这一环节的重要因素。转录因子对下游基因的调控作用,以及microRNA对转录因子的转录后调控作用是基因调控网络的重要组成部分。已报道的玉米GMS转录因子和miRNA数量较少,因为没有对花药不同发育时期进行基因组水平的综合分析,所以难以构建玉米雄性发育分子遗传的调控网络。近日,北京首佳利华科技有限公司研发团队在The Crop Journal上在线发表了题为“Genome-wide analyses on transcription factors and their potential microRNA regulators involved in maize male fertility”的研究论文。通过玉米花药发育全时期转录组测序(RNA-seq)分析,结合细胞学、生理学分析和CRISPR/Cas9基因敲除研究,发现了玉米花药发育过程中基因转录水平变化规律与细胞学和生理学变化规律的紧密对应关系。共鉴定到1087个与玉米雄性发育相关的转录因子基因、118个miRNA和99对miRNA—转录因子基因调控关系,其中ZmGAMYB是一个雄性不育转录因子的新基因。以该基因为例,通过miRNA和基因表达分析,证实zma-miR159和zma-miR319对ZmGAMYB表达有抑制作用,证明miRNA和转录因子协同调控玉米雄性发育。
首先,该研究聚焦玉米基因组中的转录因子基因,通过分析玉米自交系W23花药12个时期的RNA-seq数据,鉴定到1087个时期差异表达的转录因子基因,采用基因表达早晚模式聚类分析,把其中1079个基因分为6类。对这6类转录因子基因及其共表达或调控基因的功能进行GO和KEGG富集分析,发现基因表达水平变化与花药或花粉发育过程中细胞学和生理学变化存在对应关系。细胞周期和细胞有丝分裂相关基因在减数分裂前高表达,与该时期花药壁细胞和造孢细胞活跃的有丝分裂相对应;孢粉素合成和花粉壁形成相关基因以及氧化还原相关基因在减数分裂期间高表达,与该时期花粉壁形成过程以及活性氧积累诱导之后的绒毡层细胞凋亡(PCD)活动相符合;离子转运和跨膜转运相关基因在减数分裂后高表达,与减数分裂之后花药外壁角质和蜡质层以及花粉壁形成所需脂类物质的转运相对应;光合作用基因在减数分裂期间及之后高表达,与花药内皮层细胞叶绿体在减数分裂之后发育成熟,开始行使光合作用功能相一致。这是首次利用花药发育全生育期细胞学和生理学表型变化规律解释该发育过程相关基因功能的生物意义。
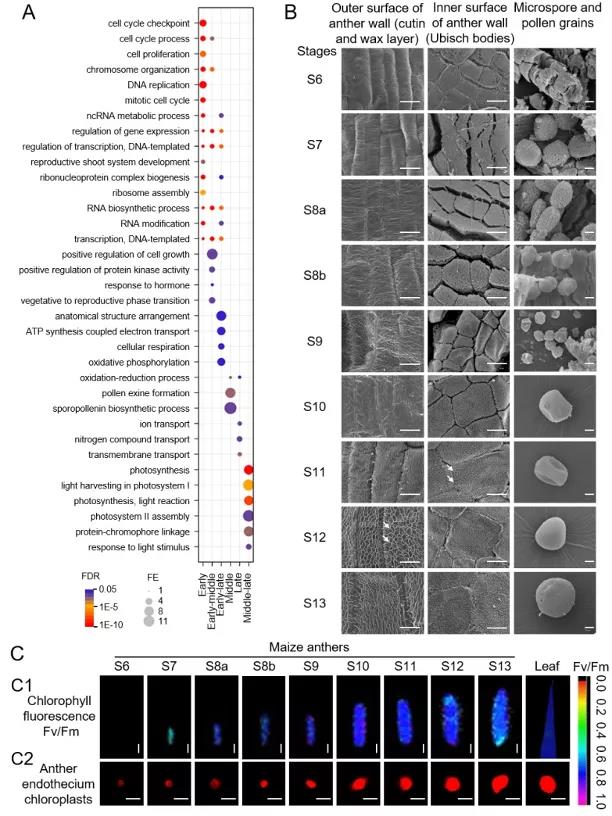
图1 玉米雄性发育过程相关基因功能聚类与细胞学和生理学变化规律的对应关系
然后,利用已发表的及本研究新测序的转录组数据,比较ocl4、ms23、ms7-6007以及lob30转录因子基因GMS突变体和野生型花药的转录组,发现上述1079个转录因子基因的绝大多数在突变体与野生型之间存在显著的差异表达。进一步分析花药miRNA测序数据,鉴定出118个时期差异表达的miRNA,这些miRNA在这4个GMS转录因子基因突变体和野生型花药之间显示不同程度的差异表达。综合分析RNA-seq和miRNA-seq数据,鉴定出99对可信度较高的miRNA—转录因子基因调控关系(图2),可归类为至少25个调控模块,其中至少10个调控模块曾被报道在玉米等植物中参与调控花药和花粉发育。

图2 99对miRNA—转录因子基因调控关系影响玉米雄性发育的分析
最后,根据CRISPR/Cas9基因敲除实验结果,发现玉米转录因子基因ZmGAMYB及其同源基因ZmGAMYB-2为新的玉米雄性不育转录因子基因。qRCR实验证实zma-miR159和zma-miR319对ZmGAMYB的表达有抑制作用(图3)。本研究鉴定了玉米雄性不育转录因子新基因,证实了转录因子基因、miRNA及miRNA—转录因子调控关系参与调节玉米花药和花粉发育过程,本研究结果丰富了玉米雄性不育候选基因资源,扩展了玉米雄性发育分子遗传调控网络信息,有助于深入解析玉米雄性不育的分子机制。
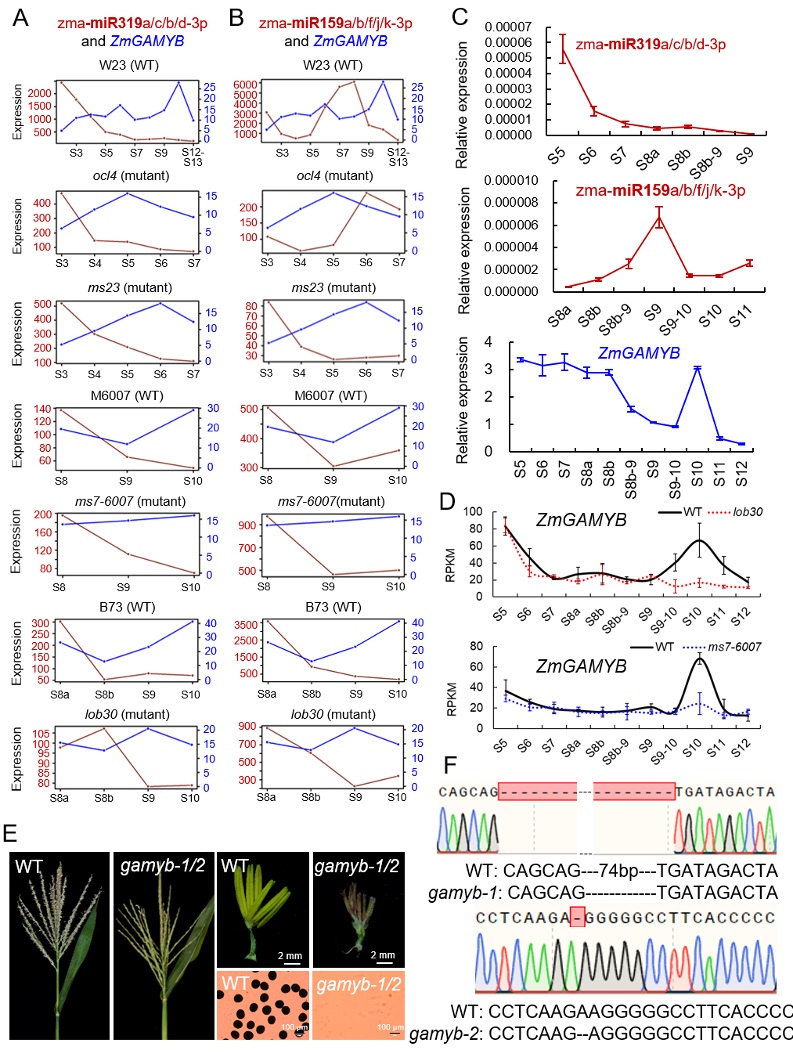
图3 zma-miR159和zma-miR319对ZmGAMYB表达的抑制作用
该研究得到国家自然科学基金项目(31771875、31971958、31871702)、中央高校基本科研业务费(2302019FRF-TP-19-013A1、06500136)和国家重点研发计划项目(017YFD0102001、2018YFD0100806、2017YFD0101201)的支持。
